신라젠, DMC 권고를 FDA에도 보고할 예정
순조롭게 진행되던 국내 바이오 기업 신라젠의 펙사벡 ‘간암 대상 글로벌 임상3상’이 임상중단이란 암초를 만났다.
신라젠은 지난 1일(현지시간) 미국 데이터모니터링위원회(DMC)와 항암 바이러스 물질 ‘펙사벡’의 간암 대상 글로벌 임상 3상에 대한 무용성 진행 평가 결과 임상 중단을 권고받았다고 밝혔다.
무용성 평가는 그동안 진행해온 ‘펙사벡’ 글로벌 임상3상의 유형성 및 안정성 등을 중간 평가하는 것을 말한다. 평가에서 특별한 문제가 없으면 기존 임상 3상이 2020년 12월 완료를 목표로 그대로 진행될 예정이었다.
한편, 신라젠은 DMC의 권고를 미국 식품의약청(FDA)에 보고할 예정이다.
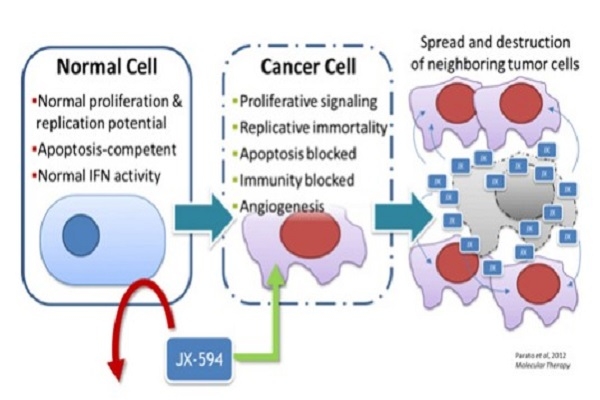
◆펙사벡이란
우두 바이러스를 유전자 재조합하여 암세포만을 선택적으로 공격하는 기전을 가지고 있는 항암 바이러스다. 주입 방법은 ‘정맥 내 투여’와 ‘종양 내 투여’가 있다.
신라젠에 따르면 현재까지 펙사벡은 약 400명의 환자에게 투여됐으며, 감기 유사 증상과 같은 경미한 정도의 부작용만 있었다.
저작권자 © CIVICNEWS(시빅뉴스) 무단전재 및 재배포 금지


